赛诺哈勃药业自主研发1类新药SNH-119014片获批开展临床试验
6月9日,倍特药业旗下赛诺哈勃药业(成都)有限公司(简称“赛诺哈勃药业”)收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,批准公司自主研发的1类化学创新药物SNH-119014片开展相应临床试验,公司将按照相关规定和计划启动I期临床研究。
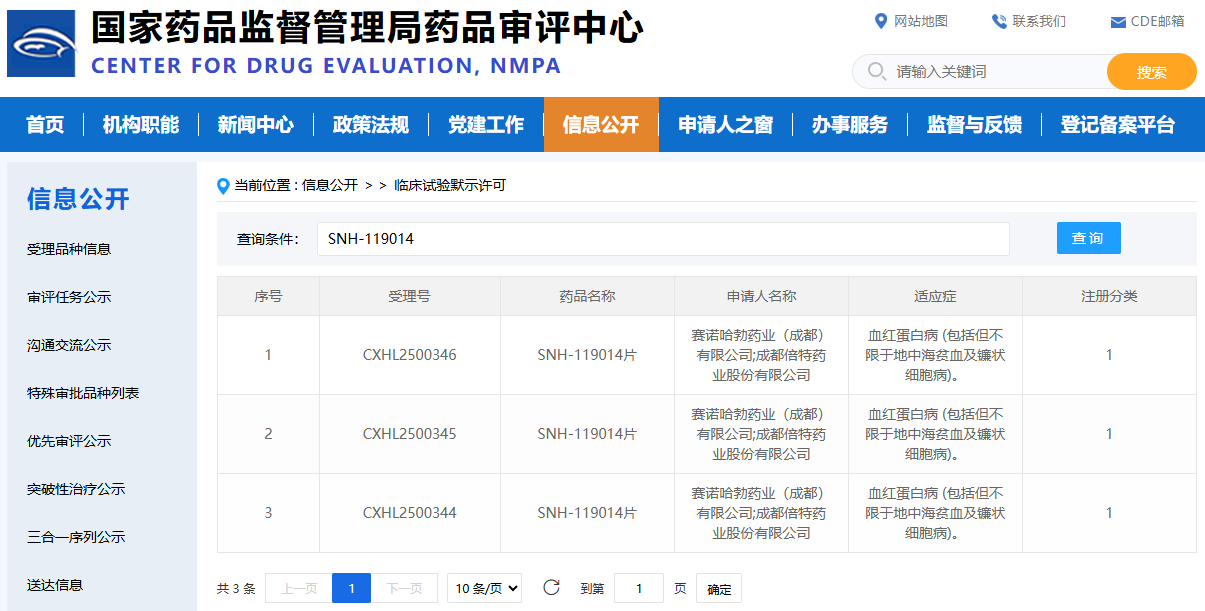
(图源:CDE)
关于SNH-119014片
SNH-119014是赛诺哈勃药业自主研发的一款全新小分子丙酮酸激酶激动剂,拟用于治疗血红蛋白病(包括但不限于地中海贫血及镰状细胞病)。本品设计开发为片剂,拟采用口服给药。
SNH-119014与靶点的结合方式及其药效,已在多项临床前研究中成功得到验证。SNH-119014可明显提高丙酮酸激酶活性,增加生物标志物腺嘌呤核苷三磷酸(ATP)水平、降低2,3-二磷酸甘油酸(2,3-DPG)含量。
关于丙酮酸激酶激动剂
丙酮酸激酶激动剂通过提高红细胞ATP水平、降低2,3-DPG含量,满足患者红细胞的能量代谢需求,有望改善贫血、提高患者生活质量[1]。业内相关领域,其在研适应症包括丙酮酸激酶缺乏症(PKD)、地中海贫血(Thalassemia,以下简称"地贫")、镰状细胞病(SCD)等。截至目前, AG-348(Mitapivat®)用于治疗PKD的适应症已获批上市;地贫适应症已完成III期临床,预估2025年获批上市;SCD适应症正在开展III期临床。FT-4202(Etavopivat®)在地贫、SCD处于临床II/III期阶段,并于2023年底获得国内新药临床申请,已完成I期临床试验。对于地贫,国内尚没有丙酮酸激酶激动剂上市。口服小分子在长期治疗中具有依从性优势,该疗法有望改善地贫患者的临床症状和生活质量。
关于血红蛋白病及治疗现状
血红蛋白病是由于血红蛋白中α或β珠蛋白基因的突变和/或缺失引起血红蛋白合成障碍或结构异常的一组遗传性血液病。常见的血红蛋白病包括地贫和其他与β珠蛋白异常氨基酸序列相关的疾病,如SCD和血红蛋白病E(HbE)[2]。
全球范围内,至少5.2%的人口携带血红蛋白病相关显著变异,每1000例受孕中有2.7例胎儿受到影响。在世界范围内,约1.5%的人口携带β-地贫基因,约5%的人口携带α-地贫基因。2021年的统计数据表明,每10万人中约有15-22例地贫患者,发病人群主要集中在地中海、中东、东南亚地区[3]。
在我国,血红蛋白病主要以地贫居多,高发于长江以南,广东、广西和海南地区,α-地贫发生率约为6.18%-15.35%,β-地贫发生率约为2.77% - 6.64%[4]。
造血干细胞移植(HSCT)和基因疗法是目前地贫的治愈性措施,但受到患者移植年龄、身体条件及相对较高治疗费用的限制,适合该疗法的患者占比很小。现有支持性手段效果有限且副作用大,患者面临巨大的经济负担和心理压力,因此对于新疗法的需求尤为迫切[5]。
目前,除铁螯合剂之外,尚无针对地贫的小分子药物获批上市。开发有效、安全、可负担的新药,可以减少患者对输血的依赖、提高生活质量、改善贫血指标,缓解因长期贫血和铁过载导致的相关并发症,延缓疾病进展。
关于赛诺哈勃药业
赛诺哈勃药业是倍特药业旗下专注于创新小分子药物研发的重要研发机构。倍特药业目前拥有在研项目超过300个,并加速推进一系列具有临床价值的药物研发和产业化进程。其中,赛诺哈勃药业研发管线已覆盖肿瘤、自身免疫性疾病、止血、罕见病等治疗领域。除此次申报的SNH-119014项目外,赛诺哈勃药业已有三个1类新药获准或正在进行临床试验,另有多个新药项目处于临床申请或临床前开发阶段。
封面图片
作者:John Lazarchick
来源:American Society of Hematology
参考文献
[1] Luo W, Semenza G L. Emerging roles of PKM2 in cell metabolism and cancer progression[J]. Trends Endocrinol Metab, 2012, 23(11): 560-6.
[2] Kohne E. Hemoglobinopathies: clinical manifestations, diagnosis, and treatment[J]. Dtsch Arztebl Int, 2011, 108(31-32): 532-40.
[3] Modell B, Darlison M. Global epidemiology of haemoglobin disorders and derived service indicators[J]. Bull World Health Organ, 2008, 86(6): 480-7.
[4] Goonasekera H W, Paththinige C S, Dissanayake V H W. Population Screening for Hemoglobinopathies[J]. Annu Rev Genomics Hum Genet, 2018, 19: 355-380.
[5] La Nasa G, Vacca A, Littera R, et al. What Unrelated Hematopoietic Stem Cell Transplantation in Thalassemia Taught us about Transplant Immunogenetics[J]. Mediterr J Hematol Infect Dis, 2016, 8(1): e2016048.






